監管藥廠
2 posters
INCA's forum :: 純聊天, 八卦, 資訊交流 :: 醫療康健
第1頁(共2頁)
 監管藥廠
監管藥廠
澳洲專家報告的建議
‧藥廠的法定授權人要通過認可訓練,但不一定為藥劑師。
‧加強突擊巡查藥廠,每間藥廠每年至少突擊巡查一次。
‧若發現藥廠有問題,藥廠必須呈交報告。
‧巡查隊伍要有連貫性,發現藥廠有問題的督察,必須負責檢視藥廠日後的改善措施。
‧藥廠需為藥物做微生物測試。
‧加強製藥員工的培訓及教育。
‧將本地GMP規格,提升至歐盟或美國的有關水平。
本港今年初爆出連串嚴重藥物事故,政府成立藥物監管制度檢討委員會,並耗資一百萬元委託澳洲專家來港視察「良好藥品生產規則」(GMP)制度後提出多項建議,包括毋須規定由藥劑師出任藥廠的法定授權人,更獲藥劑業及毒藥管理局通過。有委員會成員批評港府先斬後奏,無諮詢委員會便通過建議,又擔心藥廠無藥劑師駐場,令藥物事故有增無減,計劃明日(本月四日)到政府總部請願,要求曾蔭權正視問題。食物及衞生局承認,曾向藥劑業及毒藥管理局及委員會之下的檢討製藥工作小組介紹專家建議。委員會預計年底才完成全部檢討工作,發表最後報告。

香港醫院藥劑師協會的代表不滿當局提出取消藥劑師任藥廠授權人的建議。
據悉,委員會之下檢討製藥工作小組八月底召開會議,突接獲當局提交的澳洲專家報告,並指已獲藥劑業及毒藥管理局通過,令成員覺得被蒙在鼓裏。
其中一項建議指,因本地藥廠聘請藥劑師有困難,提議取消現行必須由藥劑師任藥廠授權人的規例,只要通過認可訓練人士便可任授權人,引起大部分成員不滿,擔心令藥廠更欠監管。
憂爆更多藥物事故
委員會成員兼執業藥劑師協會會長鄭綺雯說:「究竟呢班專家睇過乜、做過乜?我哋咩都唔知,唔能夠接受報告!點解藥廠話難請藥劑師,就唔使規定由藥劑師做授權人?我哋會去信當局反映呢個問題!」
她擔心藥廠監管「行倒車」,有機會爆出更多事故,影響公眾安全。該會聯同病人組織、醫院藥劑師協會,計劃到政府總部請願。
另有委員會成員指,大會的檢討報告預計年底才完成,但澳洲專家建議卻先被當局拍板,有先斬後奏之嫌,「咁即係當委員會無到,藥物監管應該要專業化,無藥劑師駐場,變相係降低水平,當局係咪同製藥界打籠通?」
關注病人權益的社區組織協會幹事彭鴻昌質疑為何整體檢討未完成,但澳洲專家的建議已私下通過。他認為藥廠最好有藥劑師駐場,參與重要決定及管理,避免讓商業決定主導製藥程序。
香港科研製藥聯會執行董事陳素娟則指,外國藥廠規定授權人須具製藥及管理藥廠的經驗,但無指定由哪個專業負責,除藥劑師外、微生物、化學或生物科技專家亦可出任。
‧藥廠的法定授權人要通過認可訓練,但不一定為藥劑師。
‧加強突擊巡查藥廠,每間藥廠每年至少突擊巡查一次。
‧若發現藥廠有問題,藥廠必須呈交報告。
‧巡查隊伍要有連貫性,發現藥廠有問題的督察,必須負責檢視藥廠日後的改善措施。
‧藥廠需為藥物做微生物測試。
‧加強製藥員工的培訓及教育。
‧將本地GMP規格,提升至歐盟或美國的有關水平。
本港今年初爆出連串嚴重藥物事故,政府成立藥物監管制度檢討委員會,並耗資一百萬元委託澳洲專家來港視察「良好藥品生產規則」(GMP)制度後提出多項建議,包括毋須規定由藥劑師出任藥廠的法定授權人,更獲藥劑業及毒藥管理局通過。有委員會成員批評港府先斬後奏,無諮詢委員會便通過建議,又擔心藥廠無藥劑師駐場,令藥物事故有增無減,計劃明日(本月四日)到政府總部請願,要求曾蔭權正視問題。食物及衞生局承認,曾向藥劑業及毒藥管理局及委員會之下的檢討製藥工作小組介紹專家建議。委員會預計年底才完成全部檢討工作,發表最後報告。

香港醫院藥劑師協會的代表不滿當局提出取消藥劑師任藥廠授權人的建議。
據悉,委員會之下檢討製藥工作小組八月底召開會議,突接獲當局提交的澳洲專家報告,並指已獲藥劑業及毒藥管理局通過,令成員覺得被蒙在鼓裏。
其中一項建議指,因本地藥廠聘請藥劑師有困難,提議取消現行必須由藥劑師任藥廠授權人的規例,只要通過認可訓練人士便可任授權人,引起大部分成員不滿,擔心令藥廠更欠監管。
憂爆更多藥物事故
委員會成員兼執業藥劑師協會會長鄭綺雯說:「究竟呢班專家睇過乜、做過乜?我哋咩都唔知,唔能夠接受報告!點解藥廠話難請藥劑師,就唔使規定由藥劑師做授權人?我哋會去信當局反映呢個問題!」
她擔心藥廠監管「行倒車」,有機會爆出更多事故,影響公眾安全。該會聯同病人組織、醫院藥劑師協會,計劃到政府總部請願。
另有委員會成員指,大會的檢討報告預計年底才完成,但澳洲專家建議卻先被當局拍板,有先斬後奏之嫌,「咁即係當委員會無到,藥物監管應該要專業化,無藥劑師駐場,變相係降低水平,當局係咪同製藥界打籠通?」
關注病人權益的社區組織協會幹事彭鴻昌質疑為何整體檢討未完成,但澳洲專家的建議已私下通過。他認為藥廠最好有藥劑師駐場,參與重要決定及管理,避免讓商業決定主導製藥程序。
香港科研製藥聯會執行董事陳素娟則指,外國藥廠規定授權人須具製藥及管理藥廠的經驗,但無指定由哪個專業負責,除藥劑師外、微生物、化學或生物科技專家亦可出任。

hkinca38- 訪客
 回收問題藥物倡三級制
回收問題藥物倡三級制
連串藥物事故反映本港藥物監管制度形同虛設。當局成立的藥物監管制度檢討委員會屬下製藥小組昨開會,建議本地倣效澳洲回收藥物模式,按事故嚴重性分三級處理回收藥物,可致命及致病的藥物需即時回收。
當局邀請澳洲專家來港視察本地藥管制度,建議本地參考澳洲做法,分三級處理回收問題藥物,第一級為可威脅市民性命、第二級為可令人患病、第三級為沒有對健康造成大影響。第一及第二級因影響市民安危,需立即對外公布回收詳情,並將事件通知涉及病人。本港目前並無統一的藥物回收準則,建議獲大部分小組成員同意。
專家報告又建議政府毋須要求藥廠由藥劑師任授權人,引起藥劑界及醫學界不滿,據悉與會多名代表昨強烈反對當局通過此建議,擔心藥廠在「無王管」下爆出更多事故。
促按事故嚴重性加強罰則
就加強懲處違規藥物生產商或供應商方面,本身為醫學會會長的小組成員謝鴻興指,當局應按事故嚴重性加強罰則,他批評政府無誠意檢討藥廠監管制度,沒有正視過往多宗事故的嚴重性。若當局無意提高罰則,他考慮「退會」。
當局邀請澳洲專家來港視察本地藥管制度,建議本地參考澳洲做法,分三級處理回收問題藥物,第一級為可威脅市民性命、第二級為可令人患病、第三級為沒有對健康造成大影響。第一及第二級因影響市民安危,需立即對外公布回收詳情,並將事件通知涉及病人。本港目前並無統一的藥物回收準則,建議獲大部分小組成員同意。
專家報告又建議政府毋須要求藥廠由藥劑師任授權人,引起藥劑界及醫學界不滿,據悉與會多名代表昨強烈反對當局通過此建議,擔心藥廠在「無王管」下爆出更多事故。
促按事故嚴重性加強罰則
就加強懲處違規藥物生產商或供應商方面,本身為醫學會會長的小組成員謝鴻興指,當局應按事故嚴重性加強罰則,他批評政府無誠意檢討藥廠監管制度,沒有正視過往多宗事故的嚴重性。若當局無意提高罰則,他考慮「退會」。

hkinca38- 訪客
 監管賣藥 售維他命丸都要領牌
監管賣藥 售維他命丸都要領牌
為減少藥物事故,政府成立的藥物監管制度檢討委員會完成檢討,提出 18項建議。所有售賣維他命丸、止痛藥,甚至漱口水及消毒肥皂等非毒藥藥物的零售店均要領牌;藥房所有營業時間要有藥劑師在場;非專利藥物申請註冊時,要通過臨床測試。藥業界指藥物生產成本增加或需加價一成至兩成,藥房亦稱要加價。
影響 3000間零售店
現時售賣「毒藥」類別藥物如傷風素的超市及便利店等零售及批發商才要申領該類別的藥物牌,但任何店舖甚至菜檔均可售賣含藥劑成份的「非毒藥」藥物,如維他命丸或止痛藥。委員會建議批發及零售商賣非毒藥藥物均要領牌,涉及最少 3,000間藥行、油站及雜貨店。
現時藥劑師、英國多個專業團體人士,以及藥劑業及毒藥管理局認為合資格者,均可成為藥廠授權人,為每批出廠藥物把關,但要求及責任不清晰。委員會建議提高授權人資歷要求,如藥劑師經驗由 1年增至 2年,或要持續進修。現時 25間 GMP(良好藥物生產規範)藥廠由藥劑師任授權人。
消息人士指,本港藥廠沿用 95年世界衞生組織 GMP標準,當局希望以5年時間提升至嚴格的歐盟 PIC/S標準,屆時每年每種藥物需按成份及包裝,進行最少一次穩定性測試,藥廠不達標不能繼續經營。
委員會建議非專利藥申請註冊時要進行臨床測試。另藥房由現時只需三分二營業時間要有藥劑師在場,擴大至全日。港九藥房商會理事長劉愛國表示,一名藥劑師薪酬佔藥房成本三分之一,若增加一位,或要加價。
藥價或加一至兩成
醫院藥劑師學會副主席崔俊明(圖)表示,外國有 PIC/S標準的非原廠藥較本港 GMP標準非原廠藥貴一至兩成,預料本港藥廠提升至 PIC/S後,藥價會升一至兩成。
消息人士指,今年底會向食物及衞生局提交詳細報告,再訂定落實程序。衞生署藥劑師需由現時 47人,增加最少一倍至 94人。
藥物監管制度檢討委員會部份建議
1.所有批發商及零售商包括售賣非毒藥的藥物如維他命丸、止痛藥甚至含西藥成份的漱口水及消毒肥皂,均要領牌。涉及數千間零售商如雜貨店及油站
2.所有藥物零售店營業時間要有藥劑師在場
3.批發商、零售商及醫生要書面訂購藥物及保存紀錄,避免訂藥時出錯
4.將本港藥廠 GMP水平,由現時世衞 95年標準,在 2至 3年內提升至 07年標準, 4至 5年後提升至歐盟水平
5.非無菌藥物如注射用水劑,要進行微生物測試
6.非專利藥物申請註冊時要進行臨床測試
7.從事毋須直接接觸藥物的小量包裝亦要領有包裝牌照
8.收緊擔任藥廠授權人的資格
資料來源:食衞局及消息人士
影響 3000間零售店
現時售賣「毒藥」類別藥物如傷風素的超市及便利店等零售及批發商才要申領該類別的藥物牌,但任何店舖甚至菜檔均可售賣含藥劑成份的「非毒藥」藥物,如維他命丸或止痛藥。委員會建議批發及零售商賣非毒藥藥物均要領牌,涉及最少 3,000間藥行、油站及雜貨店。
現時藥劑師、英國多個專業團體人士,以及藥劑業及毒藥管理局認為合資格者,均可成為藥廠授權人,為每批出廠藥物把關,但要求及責任不清晰。委員會建議提高授權人資歷要求,如藥劑師經驗由 1年增至 2年,或要持續進修。現時 25間 GMP(良好藥物生產規範)藥廠由藥劑師任授權人。
消息人士指,本港藥廠沿用 95年世界衞生組織 GMP標準,當局希望以5年時間提升至嚴格的歐盟 PIC/S標準,屆時每年每種藥物需按成份及包裝,進行最少一次穩定性測試,藥廠不達標不能繼續經營。
委員會建議非專利藥申請註冊時要進行臨床測試。另藥房由現時只需三分二營業時間要有藥劑師在場,擴大至全日。港九藥房商會理事長劉愛國表示,一名藥劑師薪酬佔藥房成本三分之一,若增加一位,或要加價。
藥價或加一至兩成
醫院藥劑師學會副主席崔俊明(圖)表示,外國有 PIC/S標準的非原廠藥較本港 GMP標準非原廠藥貴一至兩成,預料本港藥廠提升至 PIC/S後,藥價會升一至兩成。
消息人士指,今年底會向食物及衞生局提交詳細報告,再訂定落實程序。衞生署藥劑師需由現時 47人,增加最少一倍至 94人。
藥物監管制度檢討委員會部份建議
1.所有批發商及零售商包括售賣非毒藥的藥物如維他命丸、止痛藥甚至含西藥成份的漱口水及消毒肥皂,均要領牌。涉及數千間零售商如雜貨店及油站
2.所有藥物零售店營業時間要有藥劑師在場
3.批發商、零售商及醫生要書面訂購藥物及保存紀錄,避免訂藥時出錯
4.將本港藥廠 GMP水平,由現時世衞 95年標準,在 2至 3年內提升至 07年標準, 4至 5年後提升至歐盟水平
5.非無菌藥物如注射用水劑,要進行微生物測試
6.非專利藥物申請註冊時要進行臨床測試
7.從事毋須直接接觸藥物的小量包裝亦要領有包裝牌照
8.收緊擔任藥廠授權人的資格
資料來源:食衞局及消息人士

Min Chun- 訪客
 加強搜證 罰違規藥廠
加強搜證 罰違規藥廠
今年 3、 4月本港接連發生 10宗藥廠事故,包括琪寶製藥向醫院管理局提供未經註冊藥物,結果被判罰款 6,000元。
政府消息人士表示,違規藥廠甚少被判最高刑罰,律政司認為衞生署要更詳細向法庭解釋違規藥廠對公眾衞生危害之大,令法庭明白案件嚴重性,判處相應刑罰。
判刑與案成正比
消息人士指,藥物監管制度委員會有研究藥廠的處分,現行法例下違例藥廠最高可判罰款 10萬元及監禁 2年,再修例加重刑罰機會不大。但過去 3年違例案件一般被罰約 5,000元或判處監禁後獲緩刑。
律政司認為衞生署應加強舉證力度,令法庭的判刑與案件的嚴重性成正比。
消息指,如早前歐化藥業別嘌醇含毛霉菌事件,衞生署抽取 600多個樣本化驗搜證,最少花十多萬元。律政司建議日後若衞生署勝訴,應向藥廠取回化驗費。
政府消息人士表示,違規藥廠甚少被判最高刑罰,律政司認為衞生署要更詳細向法庭解釋違規藥廠對公眾衞生危害之大,令法庭明白案件嚴重性,判處相應刑罰。
判刑與案成正比
消息人士指,藥物監管制度委員會有研究藥廠的處分,現行法例下違例藥廠最高可判罰款 10萬元及監禁 2年,再修例加重刑罰機會不大。但過去 3年違例案件一般被罰約 5,000元或判處監禁後獲緩刑。
律政司認為衞生署應加強舉證力度,令法庭的判刑與案件的嚴重性成正比。
消息指,如早前歐化藥業別嘌醇含毛霉菌事件,衞生署抽取 600多個樣本化驗搜證,最少花十多萬元。律政司建議日後若衞生署勝訴,應向藥廠取回化驗費。

Min Chun- 訪客
 藥物監管制度檢討委員會的建議
藥物監管制度檢討委員會的建議
零售、藥房及醫生層面
售賣或批發漱口水、維他命丸及止痛藥等非毒藥藥物,如雜貨舖、油站等均須申領牌照
醫生及藥房需保存訂購藥物的書面紀錄,以便追蹤藥物來源
註冊藥房需全天候有註冊藥劑師當值
藥廠層面
將規範本地藥廠的「良好藥品生產規範」提升至國際水平
列明藥廠授權人的資格,包括履歷要求,並可由非藥劑師擔任
藥廠生產非無菌藥物,須加入微生物學監測措施
將藥物由大包裝拆細包出售亦須領取包裝牌照
政府層面
處理藥物註冊的申請由五個月縮短至兩個月
考慮向發生事故的藥廠收回抽驗藥物費用
售賣或批發漱口水、維他命丸及止痛藥等非毒藥藥物,如雜貨舖、油站等均須申領牌照
醫生及藥房需保存訂購藥物的書面紀錄,以便追蹤藥物來源
註冊藥房需全天候有註冊藥劑師當值
藥廠層面
將規範本地藥廠的「良好藥品生產規範」提升至國際水平
列明藥廠授權人的資格,包括履歷要求,並可由非藥劑師擔任
藥廠生產非無菌藥物,須加入微生物學監測措施
將藥物由大包裝拆細包出售亦須領取包裝牌照
政府層面
處理藥物註冊的申請由五個月縮短至兩個月
考慮向發生事故的藥廠收回抽驗藥物費用

hkinca38- 訪客
 射頻識別管理藥物減出錯風險
射頻識別管理藥物減出錯風險
本港近年經常發生藥物醫療事故,激發香港理工大學學生利用創新科技,研究出可改善醫療機構配藥效率,減低配錯藥風險的無線射頻識別(RFID)藥物管理系統。此外,有「香港霍金」之稱的理大電子計算學系畢業生劉曉鋒,亦以RFID技術研發出方便市民外出旅遊的航班資訊及廣告系統。

黃子傑(左)及梁家敏(右)等的藥物管理系統獲獎。
理大工業及系統工程學系學生張偉蘭、梁家敏、吳淑怡及黃子傑利用RFID技術研發出藥物管理系統。他們利用RFID技術,先把藥物資料輸入電腦系統,再把藥物放在有記錄藥物資料的識別標籤的藥樽,配藥員配藥時只需以標籤閱讀器核對藥樽,藥物資料即會在電腦顯示,能防止因只用肉眼核對而取錯藥,亦可節省時間。如取錯藥,或不同藥物之間產生排斥,電腦系統亦會發出警告。梁家敏表示,現時用人手及肉眼核對藥物資料,需時較長,亦容易出錯,希望研發系統提高配藥的準確性及速度。

黃子傑(左)及梁家敏(右)等的藥物管理系統獲獎。
理大工業及系統工程學系學生張偉蘭、梁家敏、吳淑怡及黃子傑利用RFID技術研發出藥物管理系統。他們利用RFID技術,先把藥物資料輸入電腦系統,再把藥物放在有記錄藥物資料的識別標籤的藥樽,配藥員配藥時只需以標籤閱讀器核對藥樽,藥物資料即會在電腦顯示,能防止因只用肉眼核對而取錯藥,亦可節省時間。如取錯藥,或不同藥物之間產生排斥,電腦系統亦會發出警告。梁家敏表示,現時用人手及肉眼核對藥物資料,需時較長,亦容易出錯,希望研發系統提高配藥的準確性及速度。

mmvk1- 訪客
 港人工授孕科技 管理局發牌監管
港人工授孕科技 管理局發牌監管
【明報專訊】人類生殖科技管理局是根據《人類生殖科技條例》成立,以監管提供生殖科技程序的服務、胚胎研究工作、涉及生殖科技程序或胚胎研究的已使用或準備使用的配子(生殖細胞)或胚胎的處理、儲存或棄置,以及代母安排。
管理局在2008年10月開始截至今年11月3日,共發出55個人工輔助生育中心牌照,包括40個「夫精人工授精牌照」、13個「治療牌照」、2個「研究牌照」,而東區醫院 婦產科及一間私家診所正申請「夫精人工授精牌照」仍未獲批。目前仍未有持牌治療中心獲批提供「代母」服務。
管理局在2008年10月開始截至今年11月3日,共發出55個人工輔助生育中心牌照,包括40個「夫精人工授精牌照」、13個「治療牌照」、2個「研究牌照」,而東區醫院 婦產科及一間私家診所正申請「夫精人工授精牌照」仍未獲批。目前仍未有持牌治療中心獲批提供「代母」服務。

momocha- 訪客
 逾千夫婦製試管嬰 七成失敗
逾千夫婦製試管嬰 七成失敗
【明報專訊】港人愈趨遲婚,輔助生育需求近年大增,人類生殖科技管理局首次披露的數據顯示,今年首10個月本港有逾1130對夫婦「製造」試管嬰兒,但最終七成人願望落空;接受夫精人工授精者的成功率更只得一成多。生殖醫學專家直言,科技雖然先進,但年過40女性成功懷孕機會只有約一成,借助科技生育也不能太遲。
婦年過40 懷孕機會剩一成
另外,法例雖訂明所有精子、卵子和胚胎均不能買賣,但管理局調查委員會承認,近期接獲一宗投訴,涉及「禁制訂明物質」即精子、卵子或胚胎的商業交易,個案仍在初步調查。
統計處資料顯示,本港新生嬰的母親年齡中位數已由2007年的31.4歲,再上調至31.6歲。去年全港共有2885名產婦年過40歲,當中167人是45歲或以上。仁安醫院輔助生育中心負責人龍炳樑直言,今年該院輔助生育新症多達千宗,較07年約500宗求助個案倍增,當中除了30多至40歲的港婦急於生育,內地20多歲少婦嫁予四五十歲港人後希望盡快懷孕的求助亦顯著增加。
人類生殖科技管理局(下稱管理局)今年截至10月28日,在全港7間獲批准可進行體外授精的持牌治療中心,共錄得1243宗試管嬰兒服務紀錄,當中454宗(涉443對夫婦)屬精子自由游入卵子的體外授精,成功率達32%。786宗(涉690對夫婦)屬預先揀選一精子直接注入卵子的「細胞漿內精子注入法」體外授精,成功率達27%。
將之前冷藏的胚胎解凍植入母體的「凍融胚胎移植」,則錄得624宗(涉529對夫婦),成功率29%。多達40多間診所和治療中心持牌進行的「夫精人工授精」,則錄得2511次服務記錄(涉1769名夫婦),但成功率只有12%。
質量不佳 洗精擇優
針對本港人工授精成功率只有12%,龍炳樑表示是意料之內,因人工授精乃靠男方精子游入卵子,精子質量是成孕關鍵,然而,近年不少不育個案均顯示,求助男子的精子無論質和量均不佳。管理局資料顯示,共有1729名男子須接受「洗精」服務揀選優質精子。
「試管嬰兒」成功率看來更高,但生殖醫學及婦產科專科醫生蘇偉基直言,女性一旦年過40,懷孕機會便只剩一成多,惟前來求助的女性平均年齡達40.5歲,他表示,即使借助科技生育也不能太遲。家計會 估計,本港每6對夫婦便有一對不育,蘇認為,求診阻力除了每每高達10萬元的療程費用,未必人人負擔得起,也有不少人覺得不育是禁忌不願主動求醫。
明報記者 陳佩儀
婦年過40 懷孕機會剩一成
另外,法例雖訂明所有精子、卵子和胚胎均不能買賣,但管理局調查委員會承認,近期接獲一宗投訴,涉及「禁制訂明物質」即精子、卵子或胚胎的商業交易,個案仍在初步調查。
統計處資料顯示,本港新生嬰的母親年齡中位數已由2007年的31.4歲,再上調至31.6歲。去年全港共有2885名產婦年過40歲,當中167人是45歲或以上。仁安醫院輔助生育中心負責人龍炳樑直言,今年該院輔助生育新症多達千宗,較07年約500宗求助個案倍增,當中除了30多至40歲的港婦急於生育,內地20多歲少婦嫁予四五十歲港人後希望盡快懷孕的求助亦顯著增加。
人類生殖科技管理局(下稱管理局)今年截至10月28日,在全港7間獲批准可進行體外授精的持牌治療中心,共錄得1243宗試管嬰兒服務紀錄,當中454宗(涉443對夫婦)屬精子自由游入卵子的體外授精,成功率達32%。786宗(涉690對夫婦)屬預先揀選一精子直接注入卵子的「細胞漿內精子注入法」體外授精,成功率達27%。
將之前冷藏的胚胎解凍植入母體的「凍融胚胎移植」,則錄得624宗(涉529對夫婦),成功率29%。多達40多間診所和治療中心持牌進行的「夫精人工授精」,則錄得2511次服務記錄(涉1769名夫婦),但成功率只有12%。
質量不佳 洗精擇優
針對本港人工授精成功率只有12%,龍炳樑表示是意料之內,因人工授精乃靠男方精子游入卵子,精子質量是成孕關鍵,然而,近年不少不育個案均顯示,求助男子的精子無論質和量均不佳。管理局資料顯示,共有1729名男子須接受「洗精」服務揀選優質精子。
「試管嬰兒」成功率看來更高,但生殖醫學及婦產科專科醫生蘇偉基直言,女性一旦年過40,懷孕機會便只剩一成多,惟前來求助的女性平均年齡達40.5歲,他表示,即使借助科技生育也不能太遲。家計會 估計,本港每6對夫婦便有一對不育,蘇認為,求診阻力除了每每高達10萬元的療程費用,未必人人負擔得起,也有不少人覺得不育是禁忌不願主動求醫。
明報記者 陳佩儀

mochacha- 訪客
 半生工作 中年婦恨BB 人工授孕 遇流產最傷心
半生工作 中年婦恨BB 人工授孕 遇流產最傷心
【明報專訊】從事金融業的陳女士一直忙於工作,跟丈夫結婚逾10年都未有生兒育女計劃,直至年半前,年屆39歲的她眼見同齡朋友都攜子女出席聚會,話題全圍繞「仔女經」,令她頓覺生活有些欠缺,萌生生育念頭。她一直與丈夫嘗試,又向中醫求助,每月計算日子努力「造人」,仍然無所出。
40歲終誕一女「想追多一個」
陳小姐其後得悉一名與她年紀相若的朋友,以人工授孕誕下女兒,她說﹕「她的女兒很得意可愛,於是決定試試。」她接受了排卵針注射後,抽出卵子體外受精,然後植入胚胎,首次治療14周內便流產,「那時心情很差,一直在哭,是一生人最傷心的時刻」;第二次同樣失敗,待第三次胚胎植入後,終在40歲高齡懷孕,並誕下女兒。
陳小姐直至成功懷孕前後共花約15萬元,但女兒出生一刻,覺得「好開心,好滿足」,現在已放棄金融工作,希望全職照顧女兒,更計劃半年後「追多一個」,為寶貝女兒添一個伴。
生殖醫學及婦產科專科醫生蘇偉基表示,由於40歲後懷孕機會只有一成,不少臨近「界線」夫婦均飽受精神壓力。有人為求在「最後關頭」求得一子,不惜訴諸風水、中藥等方法,有夫婦更因此鬧離婚。
蘇說,曾有接受療程的女士因為很想誕下兒女,把丈夫「逼得很緊」,兩夫婦都承受很大壓力,連性生活和婚姻也亮起紅燈,「她跟我說,再不能懷孕,連婚姻都有危機」。有求子心切的婦女更出現抑鬱、焦慮、對其他事物不感興趣等情緒問題,「每說起(還未懷孕)便眼濕濕,連見家人和朋友也感到壓力」,最終醫生把她轉介精神科醫生。也有夫婦最初一同接受治療,中途轉往領養子女,放棄人工授孕。
明報記者 曾愛盈
40歲終誕一女「想追多一個」
陳小姐其後得悉一名與她年紀相若的朋友,以人工授孕誕下女兒,她說﹕「她的女兒很得意可愛,於是決定試試。」她接受了排卵針注射後,抽出卵子體外受精,然後植入胚胎,首次治療14周內便流產,「那時心情很差,一直在哭,是一生人最傷心的時刻」;第二次同樣失敗,待第三次胚胎植入後,終在40歲高齡懷孕,並誕下女兒。
陳小姐直至成功懷孕前後共花約15萬元,但女兒出生一刻,覺得「好開心,好滿足」,現在已放棄金融工作,希望全職照顧女兒,更計劃半年後「追多一個」,為寶貝女兒添一個伴。
生殖醫學及婦產科專科醫生蘇偉基表示,由於40歲後懷孕機會只有一成,不少臨近「界線」夫婦均飽受精神壓力。有人為求在「最後關頭」求得一子,不惜訴諸風水、中藥等方法,有夫婦更因此鬧離婚。
蘇說,曾有接受療程的女士因為很想誕下兒女,把丈夫「逼得很緊」,兩夫婦都承受很大壓力,連性生活和婚姻也亮起紅燈,「她跟我說,再不能懷孕,連婚姻都有危機」。有求子心切的婦女更出現抑鬱、焦慮、對其他事物不感興趣等情緒問題,「每說起(還未懷孕)便眼濕濕,連見家人和朋友也感到壓力」,最終醫生把她轉介精神科醫生。也有夫婦最初一同接受治療,中途轉往領養子女,放棄人工授孕。
明報記者 曾愛盈

momocha- 訪客
 去年接收精子銀行 養和:至今無人捐精
去年接收精子銀行 養和:至今無人捐精
【明報專訊】今年首10個月有35名婦女共捐贈51次卵母細胞,但無人願意捐贈胚胎。去年起為家計會「精子銀行」接棒的養和醫院 說,至今無人捐精;只有一對夫婦曾作兩次胎兒性別選擇,但兩次妊娠都未能持續。
養和體外受孕中心負責人兼婦女健康及產科部主管陳煥堂直言,即使大力宣傳捐精服務,至今仍無人捐贈,「可能市民認為我們是私家醫院,捐出精子會被用來賺錢,故不甚樂意吧」。他強調,法例訂明捐精、捐卵不可作商業買賣,只能給車馬費。
家計會去年初結束「精子銀行」,並計劃把28名捐精者的精液轉交養和醫院接收,因家計會最終未能確定已獲捐精者同意把精液及個人資料轉交養和,故今年5月把全部精子庫存銷毁。
捐精卵最高補償逾千元
目前全港共有7間持牌治療中心獲批准提供儲存及捐贈精液、精子、卵母細胞或胚胎服務,根據《生殖科技及胚胎研究實務守則》,捐精和捐卵可獲「收入損失」或其他實報實銷開支補償。收入損失每天總額不得逾380元,交通開支可獲定額款項300元,捐卵者陪同人可獲300元車馬費。至於因捐贈配子(即生殖細胞)當天要找替工的額外開支,補償額為380元。
捐精者每日可獲補償總額上限1060元,捐卵者為1360元(包括陪同人的車馬費),捐卵導致的醫療開支則不設上限。目前只有瑪麗醫院和養和醫院提供選擇胎兒性別服務,只限於避免誕下法例列明的遺傳病嬰兒。
養和體外受孕中心負責人兼婦女健康及產科部主管陳煥堂直言,即使大力宣傳捐精服務,至今仍無人捐贈,「可能市民認為我們是私家醫院,捐出精子會被用來賺錢,故不甚樂意吧」。他強調,法例訂明捐精、捐卵不可作商業買賣,只能給車馬費。
家計會去年初結束「精子銀行」,並計劃把28名捐精者的精液轉交養和醫院接收,因家計會最終未能確定已獲捐精者同意把精液及個人資料轉交養和,故今年5月把全部精子庫存銷毁。
捐精卵最高補償逾千元
目前全港共有7間持牌治療中心獲批准提供儲存及捐贈精液、精子、卵母細胞或胚胎服務,根據《生殖科技及胚胎研究實務守則》,捐精和捐卵可獲「收入損失」或其他實報實銷開支補償。收入損失每天總額不得逾380元,交通開支可獲定額款項300元,捐卵者陪同人可獲300元車馬費。至於因捐贈配子(即生殖細胞)當天要找替工的額外開支,補償額為380元。
捐精者每日可獲補償總額上限1060元,捐卵者為1360元(包括陪同人的車馬費),捐卵導致的醫療開支則不設上限。目前只有瑪麗醫院和養和醫院提供選擇胎兒性別服務,只限於避免誕下法例列明的遺傳病嬰兒。

momocha- 訪客
 西藥規管不足恐危及市民
西藥規管不足恐危及市民
(明報)2009年11月25日 星期三 15:10
新一份的審計報告批評,衛生署並規管進出口西藥不力,部分流入本港市面,恐怕會危害市民的健康。
審計署報告指,衛生署每月簽發頗多進口證,讓藥物(註冊和未經註冊)進口作轉口用途,在這些進口藥物當中,部分數量龐大或價值不菲。以這種方式進口的未經註冊藥物,如在本港市場分銷作售賣或服食用途,會危害市民的健康。
然而,衛生署並無採取足夠措施,追蹤進口作轉口用途藥物的流動情況,亦沒有規定持牌藥商,就藥物流動情況提交報告表。
審計署查核衛生署簽發給海關的15張進口證,發現3張涉及進口藥物,沒有轉口到其他地方,而在本港不當出售。
審計署又發現,有9宗涉及藥物的交易,未領有進口證進口未經註冊的藥物。
審計署說,衛生署沒有特別巡查藥物批發商及進出口商,截至今年6月底,約4成的批發商及進出口商超過一年未被巡查,建議當局作出改善。
新一份的審計報告批評,衛生署並規管進出口西藥不力,部分流入本港市面,恐怕會危害市民的健康。
審計署報告指,衛生署每月簽發頗多進口證,讓藥物(註冊和未經註冊)進口作轉口用途,在這些進口藥物當中,部分數量龐大或價值不菲。以這種方式進口的未經註冊藥物,如在本港市場分銷作售賣或服食用途,會危害市民的健康。
然而,衛生署並無採取足夠措施,追蹤進口作轉口用途藥物的流動情況,亦沒有規定持牌藥商,就藥物流動情況提交報告表。
審計署查核衛生署簽發給海關的15張進口證,發現3張涉及進口藥物,沒有轉口到其他地方,而在本港不當出售。
審計署又發現,有9宗涉及藥物的交易,未領有進口證進口未經註冊的藥物。
審計署說,衛生署沒有特別巡查藥物批發商及進出口商,截至今年6月底,約4成的批發商及進出口商超過一年未被巡查,建議當局作出改善。

George H- 訪客
 假藥充斥病人隨時無命
假藥充斥病人隨時無命
假藥充斥市面,危害市民生命安全。有調查揭發,在本港購得假藥的情況相當普遍,在一般受訪者中,二成一稱曾購得或懷疑購得假藥,而長期病患受訪者的「中招」比率更高達四成;有病人組織指假藥會危害服用者生命,批評當局未夠重視假藥的遺害,致打擊不力,質疑當局自○五年至今只破獲廿八宗販售假藥個案數字偏低,未能反映現實,估實際個案較破案數字高出一百倍,建議政府加重罰則及制訂獨立法例針對販售假藥問題。
病人互助組織聯盟上月委託港大民意研究計劃訪問了約一千名市民,及一百六十八名長期病患者,結果發現近兩成一受訪市民,及四成受訪病友曾購得假藥或懷疑購得假藥,假藥主要包括藥油、感冒藥、血壓藥及心臟病藥等。
有藥物代理商指,一些在內地享有知名度的品牌藥物,是不法之徒的主要目標,以吸引訪港內地旅客購買。
缺監管檢控不力
至於為何假藥充斥本港市面,四成受訪的病友認為原因是基於政府監管不足、檢控不力與刑罰過輕等三個因素同時導致;而一般受訪者抱有相類看法的比率更高,接近五成。
聯盟主席曾建平指,假藥問題近年愈趨嚴重,而病人若服用假藥,可能危害生命安全,令其延誤診治,後果嚴重,但政府只以管制一般貨品的《商品說明條例》來檢控販售假藥的不法商人,未有針對打擊假藥制訂獨立法例,顯然對問題未夠重視。
刑罰過輕欠阻嚇
法律界人士梁丙焄補充,現時本港販售假藥的刑罰偏低,主要是判監禁緩刑,罰款額亦僅數千元,阻嚇性不足。她又指,部分售假藥的藥房東主在屢犯後,會把藥房結業以逃避刑責,很快又以新名字開設新藥房繼續經營,建議政府加強執法與加重刑罰以收阻嚇作用。
海關版權及商標調查科高級監督何仕景則稱,今年以放蛇方式在藥房購得假藥的比例有輕微下跌之勢,由去年約百分之七機會購得假藥,降至今年約百分之六;又指過去五年,海關與衞生署合作破獲的賣假藥個案共有二十八宗。
不過,曾建平直指破案數字少,不等於假藥問題不嚴重,因為市民有可能「食咗假藥都唔知」,而未有向海關舉報,估計販售假藥的實際個案可能會較破案數字高一百倍。
病人互助組織聯盟上月委託港大民意研究計劃訪問了約一千名市民,及一百六十八名長期病患者,結果發現近兩成一受訪市民,及四成受訪病友曾購得假藥或懷疑購得假藥,假藥主要包括藥油、感冒藥、血壓藥及心臟病藥等。
有藥物代理商指,一些在內地享有知名度的品牌藥物,是不法之徒的主要目標,以吸引訪港內地旅客購買。
缺監管檢控不力
至於為何假藥充斥本港市面,四成受訪的病友認為原因是基於政府監管不足、檢控不力與刑罰過輕等三個因素同時導致;而一般受訪者抱有相類看法的比率更高,接近五成。
聯盟主席曾建平指,假藥問題近年愈趨嚴重,而病人若服用假藥,可能危害生命安全,令其延誤診治,後果嚴重,但政府只以管制一般貨品的《商品說明條例》來檢控販售假藥的不法商人,未有針對打擊假藥制訂獨立法例,顯然對問題未夠重視。
刑罰過輕欠阻嚇
法律界人士梁丙焄補充,現時本港販售假藥的刑罰偏低,主要是判監禁緩刑,罰款額亦僅數千元,阻嚇性不足。她又指,部分售假藥的藥房東主在屢犯後,會把藥房結業以逃避刑責,很快又以新名字開設新藥房繼續經營,建議政府加強執法與加重刑罰以收阻嚇作用。
海關版權及商標調查科高級監督何仕景則稱,今年以放蛇方式在藥房購得假藥的比例有輕微下跌之勢,由去年約百分之七機會購得假藥,降至今年約百分之六;又指過去五年,海關與衞生署合作破獲的賣假藥個案共有二十八宗。
不過,曾建平直指破案數字少,不等於假藥問題不嚴重,因為市民有可能「食咗假藥都唔知」,而未有向海關舉報,估計販售假藥的實際個案可能會較破案數字高一百倍。

Dino- 文章數 : 951
注冊日期 : 2009-12-02
 製藥規範倡5年達歐盟標準 小型「山寨廠」料遭淘汰
製藥規範倡5年達歐盟標準 小型「山寨廠」料遭淘汰
【明報專訊】本港年初接連揭發10宗藥劑製品事故,但衛生署最新資料顯示,其中3宗違規個案,包括生產發霉藥的偉民藥廠亦不被起訴。藥物監管制度檢討委員會本月30日會召開最後一次會議,當局已就委員會多項建議訂定落實時間表,五六年內將藥廠的「良好藥品生產規範」(GMP)水平推上國際級,小規模「山寨廠」無可避免被淘汰。
10藥物事故 僅4藥商定罪
藥物事故成今年焦點,衛署檢控個案亦較去年增加,但連同歐化藥業在內,只有4間涉事故藥業被定罪,罰款5000至20萬元不等,3間藥業即使出售未經註冊藥,甚至生產疑受黴菌污染利尿藥的歐化系偉民藥廠,也因律政司 不建議起訴而毋須面對法律制裁(見表)。
政府委任的藥物監管制度檢討委員會大致完成最後報告,下周三開會後便會將報告提交食物及衛生局長,然後向公眾發表。委員會認為,最優先要執行的事項,除了藥廠生產藥物須引入微生物測試標準外,日後所有非原廠藥必須備有生體可用率和等效率研究報告,才可在本港註冊出售,建議明年盡快成立「專家建議委員會」,審閱生體可用率和生體等效率研究文件。
藥劑師全日駐藥房 短期難實施
衛生署資料顯示,本港註冊的1.95萬種藥劑製品中,多達1.8萬種屬非原廠藥物,香港製藥商會會長鄭香郡指出,註冊藥物補交報告需時,料當局會按風險分批做,如癲癇藥、血壓藥等先行,維他命等低風險藥物或較遲。
至於三大改革︰要求藥房全日有藥劑師駐場、售賣非毒藥藥品商戶須領牌、醫生和零售商須保存訂藥書面紀錄以備追查藥物去向,因牽連甚廣並涉及修例,當局最快2011年才能向立法會提交修例草案,短期內難實施。
以目前全港有511間藥房估計,全日有藥劑師的額外人手需求約250人,以中大和港大每年培訓50名藥劑師計算,也需5年才達標;全港藥品商戶領牌前,不排除先以自願登記作行政規管。
至於提升本地藥廠GMP水平的目標,初步訂於2至3年提升至2007年標準,其後在4至5年內提升至歐盟 PICS標準。有委員透露,當局預料較細規模藥廠將面臨淘汰,鄭香郡則指業界對提升水平反應積極,不排除小規模廠會透過合併增強實力。
明報記者 陳佩儀
10藥物事故 僅4藥商定罪
藥物事故成今年焦點,衛署檢控個案亦較去年增加,但連同歐化藥業在內,只有4間涉事故藥業被定罪,罰款5000至20萬元不等,3間藥業即使出售未經註冊藥,甚至生產疑受黴菌污染利尿藥的歐化系偉民藥廠,也因律政司 不建議起訴而毋須面對法律制裁(見表)。
政府委任的藥物監管制度檢討委員會大致完成最後報告,下周三開會後便會將報告提交食物及衛生局長,然後向公眾發表。委員會認為,最優先要執行的事項,除了藥廠生產藥物須引入微生物測試標準外,日後所有非原廠藥必須備有生體可用率和等效率研究報告,才可在本港註冊出售,建議明年盡快成立「專家建議委員會」,審閱生體可用率和生體等效率研究文件。
藥劑師全日駐藥房 短期難實施
衛生署資料顯示,本港註冊的1.95萬種藥劑製品中,多達1.8萬種屬非原廠藥物,香港製藥商會會長鄭香郡指出,註冊藥物補交報告需時,料當局會按風險分批做,如癲癇藥、血壓藥等先行,維他命等低風險藥物或較遲。
至於三大改革︰要求藥房全日有藥劑師駐場、售賣非毒藥藥品商戶須領牌、醫生和零售商須保存訂藥書面紀錄以備追查藥物去向,因牽連甚廣並涉及修例,當局最快2011年才能向立法會提交修例草案,短期內難實施。
以目前全港有511間藥房估計,全日有藥劑師的額外人手需求約250人,以中大和港大每年培訓50名藥劑師計算,也需5年才達標;全港藥品商戶領牌前,不排除先以自願登記作行政規管。
至於提升本地藥廠GMP水平的目標,初步訂於2至3年提升至2007年標準,其後在4至5年內提升至歐盟 PICS標準。有委員透露,當局預料較細規模藥廠將面臨淘汰,鄭香郡則指業界對提升水平反應積極,不排除小規模廠會透過合併增強實力。
明報記者 陳佩儀

Dino- 文章數 : 951
注冊日期 : 2009-12-02
 含西布曲明藥物應小心使用
含西布曲明藥物應小心使用
(明報)2010年1月22日 星期五 22:15
衛生署基於最新研究結果,今日提醒市民安全使用含有「西布曲明」成分的藥物。
衛生署稱,歐盟藥物管理機構(European Medicines Agency)基於最新研究結果,認為服用「西布曲明」所帶來的風險較其好處為高,該組織轄下的人用藥物委員會建議終止含有「西布曲明」藥物的銷售權。
發言人表示,美國食物及藥物管理局研究有關研究數據後,要求製造商在產品標籤加上新的忌用字句,列明患有心血管疾病的人士不能服用「西布曲明」,而心血管疾病包括冠狀動脈病、中風或短暫性腦缺血、心律不齊、充血性心衰竭、末稍動脈病症和未受控制的高血壓。
美國食物及藥物管理局將會稍後完成全面的檢討,並會召開會議以決定是否需要增加規管行動,從而確保使用這些藥物的安全。
在香港,衛生署已嚴肅考慮可能出現的副作用及需求情況,並即時就含「西布曲明」的藥物進行風險評估。
發言人表示,共有40款註冊藥物含「西布曲明」,全為處方藥物。現時產品說明書已包含註明警告字句,闡明患冠心病、充血性心衰竭、心律不齊及中風的病人不應服用該等藥物。
藥劑業及毒藥管理局的註冊委員將在二月初的會議上研究有關數據。
「西布曲明」是一種用於抑壓食慾的西藥,其副作用包括導致血壓上升及心跳加劇,精神異常和可能痙攣,有心臟病 的人士不應服用。
發言人建議正在使用該藥物的市民,應諮詢醫生意見是否應繼續服用含「西布曲明」的藥物,並如在診療期間遇上任何問題,應即通知醫生。
市民如要控制體重,應注意均衡飲食及做適量運動。市民不應自行服用處方藥物,而在服用藥物以減低體重前,亦應先諮詢醫護人士的意見。
衛生署基於最新研究結果,今日提醒市民安全使用含有「西布曲明」成分的藥物。
衛生署稱,歐盟藥物管理機構(European Medicines Agency)基於最新研究結果,認為服用「西布曲明」所帶來的風險較其好處為高,該組織轄下的人用藥物委員會建議終止含有「西布曲明」藥物的銷售權。
發言人表示,美國食物及藥物管理局研究有關研究數據後,要求製造商在產品標籤加上新的忌用字句,列明患有心血管疾病的人士不能服用「西布曲明」,而心血管疾病包括冠狀動脈病、中風或短暫性腦缺血、心律不齊、充血性心衰竭、末稍動脈病症和未受控制的高血壓。
美國食物及藥物管理局將會稍後完成全面的檢討,並會召開會議以決定是否需要增加規管行動,從而確保使用這些藥物的安全。
在香港,衛生署已嚴肅考慮可能出現的副作用及需求情況,並即時就含「西布曲明」的藥物進行風險評估。
發言人表示,共有40款註冊藥物含「西布曲明」,全為處方藥物。現時產品說明書已包含註明警告字句,闡明患冠心病、充血性心衰竭、心律不齊及中風的病人不應服用該等藥物。
藥劑業及毒藥管理局的註冊委員將在二月初的會議上研究有關數據。
「西布曲明」是一種用於抑壓食慾的西藥,其副作用包括導致血壓上升及心跳加劇,精神異常和可能痙攣,有心臟病 的人士不應服用。
發言人建議正在使用該藥物的市民,應諮詢醫生意見是否應繼續服用含「西布曲明」的藥物,並如在診療期間遇上任何問題,應即通知醫生。
市民如要控制體重,應注意均衡飲食及做適量運動。市民不應自行服用處方藥物,而在服用藥物以減低體重前,亦應先諮詢醫護人士的意見。

mudu- 訪客
 中藥廠七成山寨衞署懶取締
中藥廠七成山寨衞署懶取締
全港約五百間中成藥製造商中,近七成共三百四十三間只獲過渡證明書,即未達正式註冊資格。本報發現,部分製造商登記的地址竟是住宅或居屋單位,其中一間報稱藥廠更已變為社區學院,「廠去樓空」,資料未更新。衞生署承認,中成藥製造商必須遷往符合製藥規模的非住宅處所才可獲正式註冊,但過渡性註冊已長達七年,該署仍未落實何時終結過渡期,有關注團體批評衞生署多年來不聞不問。

不少中成藥廠屬家族式經營,仍以人手加工包裝。
在中醫藥管理委員會網頁內三百四十三間「過渡性領牌中成藥製造商」中,有三間登記地址為居屋單位,記者上門查看,一間位於深水埗和一間位於香港仔的「藥廠」無人應門;另一間位於深水埗居屋單位的「藥廠」住有一名婆婆,她稱前業主是老中醫,約三、四年前已遷出,她不知所住單位是中成藥製造商。此外,部分藥廠設於舊式大廈,一間報稱位於深水埗麗閣邨商場的「藥廠」已變成社區學院。

報稱位於深水埗西九龍中心的中藥廠已人去樓空。
過渡期終結無期
衞生署○三年四月實施中藥業發牌制度,在二○○○年一月三日已營業的藥廠可申請過渡性註冊,之後開業的必須申領正式註冊牌照才可經營。該署表示,中藥組負責審批中藥商過渡證明書轉正式牌照的申請,考慮因素包括處所類型、環境和設備等,若廠房位於住宅單位,包括居屋、公屋或私人屋苑,不會獲接納。如巡查時發現廠房地址與過渡性證明書不符,會與持牌人跟進,如廠房已結業,則會拒絕申請。該署助理署長趙佩燕承認,至今未決定過渡期何時終結,只表示會考慮盡快完成過渡性註冊程序。
全民健康動力主席勞永樂醫生指出,不少中成藥製造廠「用個電飯煲嚟製藥」,衞生署明知此種情況存在多年,但「一直唔想理」,保濟丸出事後才補鑊全面巡查。他質疑,衞生署人員到住宅單位巡查,看到「山寨廠」的運作,不知從何入手。他認為,衞生署應就過渡性註冊定下時間表,正式結束過渡期,取締不合格藥廠,確保中成藥品質安全可靠。
香港藥行商會理事長黃炳明承認,不少中成藥製藥廠環境惡劣,但業界已積極改善,惟因資金問題,未能達到中成藥生產質量管理規範(GMP)。他要求當局協助有困難的業界改善廠房環境,否則本港大部分老字號中成藥廠從此結業。

不少中成藥廠屬家族式經營,仍以人手加工包裝。
在中醫藥管理委員會網頁內三百四十三間「過渡性領牌中成藥製造商」中,有三間登記地址為居屋單位,記者上門查看,一間位於深水埗和一間位於香港仔的「藥廠」無人應門;另一間位於深水埗居屋單位的「藥廠」住有一名婆婆,她稱前業主是老中醫,約三、四年前已遷出,她不知所住單位是中成藥製造商。此外,部分藥廠設於舊式大廈,一間報稱位於深水埗麗閣邨商場的「藥廠」已變成社區學院。

報稱位於深水埗西九龍中心的中藥廠已人去樓空。
過渡期終結無期
衞生署○三年四月實施中藥業發牌制度,在二○○○年一月三日已營業的藥廠可申請過渡性註冊,之後開業的必須申領正式註冊牌照才可經營。該署表示,中藥組負責審批中藥商過渡證明書轉正式牌照的申請,考慮因素包括處所類型、環境和設備等,若廠房位於住宅單位,包括居屋、公屋或私人屋苑,不會獲接納。如巡查時發現廠房地址與過渡性證明書不符,會與持牌人跟進,如廠房已結業,則會拒絕申請。該署助理署長趙佩燕承認,至今未決定過渡期何時終結,只表示會考慮盡快完成過渡性註冊程序。
全民健康動力主席勞永樂醫生指出,不少中成藥製造廠「用個電飯煲嚟製藥」,衞生署明知此種情況存在多年,但「一直唔想理」,保濟丸出事後才補鑊全面巡查。他質疑,衞生署人員到住宅單位巡查,看到「山寨廠」的運作,不知從何入手。他認為,衞生署應就過渡性註冊定下時間表,正式結束過渡期,取締不合格藥廠,確保中成藥品質安全可靠。
香港藥行商會理事長黃炳明承認,不少中成藥製藥廠環境惡劣,但業界已積極改善,惟因資金問題,未能達到中成藥生產質量管理規範(GMP)。他要求當局協助有困難的業界改善廠房環境,否則本港大部分老字號中成藥廠從此結業。

KateBush- 訪客
 業界嘆GMP門檻過高
業界嘆GMP門檻過高
有只獲過渡性註冊的老字號藥廠坦言,不少藥廠資金有限,若要提升水平至GMP認證需作龐大投資,未必能應付,但認為品質監控嚴謹,有信心通過衞署巡查。

不少老字號中成藥廠屬家族式經營,若要達到正式持牌及GMP標準,成本將大增。
本港僅七間中成藥製造商獲衞生署頒發GMP(生產質量管理規範),創立逾大半個世紀的老字號藥廠負責人何先生稱,該廠雖未獲GMP,但五、六年前已着手籌備,並已花七十多萬元進行檢驗,「我哋屬家族式經營,資金唔多,若要達標起碼要額外投資七至八百萬元,呢行規管愈來愈多,原材料又貴咗。」

中成藥製造商維特健靈每批原材料都經化驗才用來製藥,確保質素達標。
有信心過衞署一關
他無奈稱,當局只顧推行GMP,未有計劃如何資助業界,相信只有少於百分之一的藥廠可承受成本壓力,若強硬推行只會令大量藥廠面臨結業。他強調,其藥廠雖未達標,但生產至包裝等過程一手包辦,嚴格監控衞生情況,有信心能通過當局巡查。
九八年獲GMP認證的維特健靈大藥廠,董事長陳曦齡透露,當年投資五千萬元裝修、聘請英國專家,又參照世衞及英國的GMP規格才能達標,她建議中成藥製造商可以合併方式營運以減輕成本。○六年獲GMP的和興白花油藥廠有限公司,執行董事及營運總監邱禮菁認為,衞生署長遠應要求所有中成藥製造商獲GMP,提升行業規範和認受性。

不少老字號中成藥廠屬家族式經營,若要達到正式持牌及GMP標準,成本將大增。
本港僅七間中成藥製造商獲衞生署頒發GMP(生產質量管理規範),創立逾大半個世紀的老字號藥廠負責人何先生稱,該廠雖未獲GMP,但五、六年前已着手籌備,並已花七十多萬元進行檢驗,「我哋屬家族式經營,資金唔多,若要達標起碼要額外投資七至八百萬元,呢行規管愈來愈多,原材料又貴咗。」

中成藥製造商維特健靈每批原材料都經化驗才用來製藥,確保質素達標。
有信心過衞署一關
他無奈稱,當局只顧推行GMP,未有計劃如何資助業界,相信只有少於百分之一的藥廠可承受成本壓力,若強硬推行只會令大量藥廠面臨結業。他強調,其藥廠雖未達標,但生產至包裝等過程一手包辦,嚴格監控衞生情況,有信心能通過當局巡查。
九八年獲GMP認證的維特健靈大藥廠,董事長陳曦齡透露,當年投資五千萬元裝修、聘請英國專家,又參照世衞及英國的GMP規格才能達標,她建議中成藥製造商可以合併方式營運以減輕成本。○六年獲GMP的和興白花油藥廠有限公司,執行董事及營運總監邱禮菁認為,衞生署長遠應要求所有中成藥製造商獲GMP,提升行業規範和認受性。

KateBush- 訪客
 住宅及舊樓藥廠 須搬遷或結業
住宅及舊樓藥廠 須搬遷或結業
衞生署早前發現保濟丸事件涉及內地不明藥廠,署方昨指出,有理由相信藥廠管理出現問題,涉及監控人員。本港部份環境欠佳的藥廠位於住宅及舊樓,署方已要求有關廠房搬遷或結業。

保濟丸成份出錯疑是原材料受污染, 衞署昨表示有理由相信李眾勝堂管理及監控人員出問題。
將巡查全港中藥廠
衞生署助理署長趙佩燕昨接受傳媒訪問時表示,署方去年底已初步視察了全港 350間過渡性註冊藥廠,特別檢視場地及儀器是否合格,發現部份場地位於住宅及舊樓,已要求廠商搬遷或結業。署方也在市面抽樣或到廠商取樣化驗,去年共檢驗 2,700個樣本,三分一為過渡性註冊藥廠的中成藥。趙佩燕稱將巡查全港約五百間中成藥製造商,範圍包括製造紀錄、場地是否合適及監控人員質素。
保濟丸事件由新加坡當局揭發,趙佩燕解釋,當地儀器可以發現保濟丸有特別成份,進一步檢驗才發現問題,技術與本港不同,將要求本港化驗所跟進。香港醫院藥劑師學會副會長崔俊明指出,使用化學成份圖譜可顯示中成藥成份是否統一,發現有異即可重點檢測有關產品含哪些西藥成份。
政府未推國際認證
保濟丸事件源於原材料受污染。據了解, GMP認證雖規範生產流程,但不涉及儲存及運送。世界 衞生組織認可的 GSDP( Good Storage and Distribution Practice)認證為優良儲存及分發規範,確保獨立運送,避免藥物與其他貨品交叉污染,本港只有數間中成藥商或其外判運送公司有此認證。本港也有不少製造商未能為每批產品執行安全測試,或有關實驗室獲國際認證。港府也知悉上述情況,但沒有推出相關措施。
中醫藥管理委員會的資料顯示,目前只有七間中成藥製造商獲本港 GMP認證。向公立醫院提供中藥產品的農本方總經理陳隆生向本報表示,該品牌在本港沒有設廠,因此毋須申請本港 GMP認證。該品牌的廠房位於廣西南寧,屬培力藥業旗下,獲內地國家級 GMP認證,也獲美國 GMP及香港承認,「我哋產品唔平,如果冇 GMP,醫管局都唔會揀我哋。我哋嘅品質,冇對手可以做到。」他又指,該品牌已購買產品責任保險,若有人服食其產品後嚴重影響健康,可獲賠償。

保濟丸成份出錯疑是原材料受污染, 衞署昨表示有理由相信李眾勝堂管理及監控人員出問題。
將巡查全港中藥廠
衞生署助理署長趙佩燕昨接受傳媒訪問時表示,署方去年底已初步視察了全港 350間過渡性註冊藥廠,特別檢視場地及儀器是否合格,發現部份場地位於住宅及舊樓,已要求廠商搬遷或結業。署方也在市面抽樣或到廠商取樣化驗,去年共檢驗 2,700個樣本,三分一為過渡性註冊藥廠的中成藥。趙佩燕稱將巡查全港約五百間中成藥製造商,範圍包括製造紀錄、場地是否合適及監控人員質素。
保濟丸事件由新加坡當局揭發,趙佩燕解釋,當地儀器可以發現保濟丸有特別成份,進一步檢驗才發現問題,技術與本港不同,將要求本港化驗所跟進。香港醫院藥劑師學會副會長崔俊明指出,使用化學成份圖譜可顯示中成藥成份是否統一,發現有異即可重點檢測有關產品含哪些西藥成份。
政府未推國際認證
保濟丸事件源於原材料受污染。據了解, GMP認證雖規範生產流程,但不涉及儲存及運送。世界 衞生組織認可的 GSDP( Good Storage and Distribution Practice)認證為優良儲存及分發規範,確保獨立運送,避免藥物與其他貨品交叉污染,本港只有數間中成藥商或其外判運送公司有此認證。本港也有不少製造商未能為每批產品執行安全測試,或有關實驗室獲國際認證。港府也知悉上述情況,但沒有推出相關措施。
中醫藥管理委員會的資料顯示,目前只有七間中成藥製造商獲本港 GMP認證。向公立醫院提供中藥產品的農本方總經理陳隆生向本報表示,該品牌在本港沒有設廠,因此毋須申請本港 GMP認證。該品牌的廠房位於廣西南寧,屬培力藥業旗下,獲內地國家級 GMP認證,也獲美國 GMP及香港承認,「我哋產品唔平,如果冇 GMP,醫管局都唔會揀我哋。我哋嘅品質,冇對手可以做到。」他又指,該品牌已購買產品責任保險,若有人服食其產品後嚴重影響健康,可獲賠償。

KateBush- 訪客
 油塘工廈「山寨藥廠」被釘牌 衛署令舊廈民居藥廠搬遷
油塘工廈「山寨藥廠」被釘牌 衛署令舊廈民居藥廠搬遷
【明報專訊】本港不少「山寨」中藥廠隱藏於舊區唐樓,個別藥廠甚至設於市區屋苑大廈,衛生署承認情况令人關注,並已去信要求部分相關中藥廠搬遷改善,若問題持續或要考慮結業,中醫藥管理委員會中藥組更剛於上周五,裁定一間位於油塘工業大廈的「山寨廠」環境衛生欠佳,要撤銷「過渡證明書」。
被撤銷牌照的中成藥廠「非凡公司(1929)」,位於油塘工業大廈,與機器廠為鄰,負責人李迪成昨接受本報查詢時承認,該廠房原本是生產製藥廠的機器,只是「順便製埋藥」,坦言環境衛生條件「不合適」,故他們早已將藥方外判予香港一間GMP製藥廠生產。
藥廠: 原生產機器 順便製藥
他認為,該公司原來須接受聆訊的案件只涉售賣過期藥,但衛生署卻「重手」將其藥廠牌照撤銷,並不公允,故他亦準備上訴。
「過渡」中藥廠 四成於工廈
本報翻查全港343間未能申領正式牌照、只領有過渡證明書的中藥廠資料,發現約四成位於工業大廈(見表),當中包括一些較簡陋的舊式工廈,令人關注的是,位於港、九區的中藥廠不少隱藏在舊區唐樓,夾雜各類商業和民居,其中「利群中醫」製藥廠廠房甚至在牛頭角 屋苑「得寶花園B座37樓」、「香港仙草葯品公司」廠房則設於香港南區「嘉隆苑嘉俊閣17樓9室」。
衛生署容許「過渡性」藥業在屋苑設廠令人費解,助理署長趙佩燕坦言,衛署也很關注「過渡性中藥廠」場地、儀器和製藥人資歷是否適合,去年署方一次過巡視全部343間過渡藥廠,並已去信要求位於舊式唐樓和住宅等地點不當的廠房,考慮是否要搬,若問題持續或要考慮結業。但衛生署向多少間中成藥廠發出了搬遷指示,發言人卻說未能提供實際數據。
發言人補充,如處所作為住宅用途,如居民、公屋或私人屋苑單位等,不會被接納作為申請經營中成藥廠房的地址,若藥廠經營環境衛生惡劣,中藥組亦可吊銷其牌照。趙佩燕說,去年抽樣檢驗2700個中成藥樣本,其中三分一是由過渡藥廠製造。
明報記者 陳佩儀
被撤銷牌照的中成藥廠「非凡公司(1929)」,位於油塘工業大廈,與機器廠為鄰,負責人李迪成昨接受本報查詢時承認,該廠房原本是生產製藥廠的機器,只是「順便製埋藥」,坦言環境衛生條件「不合適」,故他們早已將藥方外判予香港一間GMP製藥廠生產。
藥廠: 原生產機器 順便製藥
他認為,該公司原來須接受聆訊的案件只涉售賣過期藥,但衛生署卻「重手」將其藥廠牌照撤銷,並不公允,故他亦準備上訴。
「過渡」中藥廠 四成於工廈
本報翻查全港343間未能申領正式牌照、只領有過渡證明書的中藥廠資料,發現約四成位於工業大廈(見表),當中包括一些較簡陋的舊式工廈,令人關注的是,位於港、九區的中藥廠不少隱藏在舊區唐樓,夾雜各類商業和民居,其中「利群中醫」製藥廠廠房甚至在牛頭角 屋苑「得寶花園B座37樓」、「香港仙草葯品公司」廠房則設於香港南區「嘉隆苑嘉俊閣17樓9室」。
衛生署容許「過渡性」藥業在屋苑設廠令人費解,助理署長趙佩燕坦言,衛署也很關注「過渡性中藥廠」場地、儀器和製藥人資歷是否適合,去年署方一次過巡視全部343間過渡藥廠,並已去信要求位於舊式唐樓和住宅等地點不當的廠房,考慮是否要搬,若問題持續或要考慮結業。但衛生署向多少間中成藥廠發出了搬遷指示,發言人卻說未能提供實際數據。
發言人補充,如處所作為住宅用途,如居民、公屋或私人屋苑單位等,不會被接納作為申請經營中成藥廠房的地址,若藥廠經營環境衛生惡劣,中藥組亦可吊銷其牌照。趙佩燕說,去年抽樣檢驗2700個中成藥樣本,其中三分一是由過渡藥廠製造。
明報記者 陳佩儀

hkinca38- 訪客
 英國擬監管中醫中藥
英國擬監管中醫中藥
(明報)2010年4月2日 星期五 20:25
英國政府擬立法監管售賣未註冊藥物的店舖、診所、執業人員,中醫師等另類治療人員將首當其衝。
英國沒有監管中草藥等治療方法,政府備受批評,有人更因誤服中成藥死亡。
英國政府建議規定所有提供未註冊藥物的店舖及人員,必須向補充療法及自然健康療法理事會註冊,證明執業者有足夠訓練和經驗,有關人士亦要遵守守則及購買保險。
英國政府擬立法監管售賣未註冊藥物的店舖、診所、執業人員,中醫師等另類治療人員將首當其衝。
英國沒有監管中草藥等治療方法,政府備受批評,有人更因誤服中成藥死亡。
英國政府建議規定所有提供未註冊藥物的店舖及人員,必須向補充療法及自然健康療法理事會註冊,證明執業者有足夠訓練和經驗,有關人士亦要遵守守則及購買保險。

Smart- 訪客
 黑心膠囊藥流入港府懶理
黑心膠囊藥流入港府懶理
自爆出保濟丸事件後,中成藥問題愈揭愈多。台灣近日全面掃蕩黑心藥廠,檢獲黑心膠囊逾一百一十萬顆及十五公噸假中藥粉,其中包括銀杏葉萃物、藍莓素和姬松茸膠囊等港人熟悉的產品。相對台灣的迅速取締問題藥品行動,港府對問題藥品的監管,仍處於講多過做的階段,不排除黑心保健產品早已流入本港市場出售。

台調查局分別查獲一百一十六萬顆黑心膠囊及十五公噸偽中藥粉末。 (本報台北傳真)
台灣衞生署食品藥物管理局表示,近日在全台展開偽藥行動,並於二十三家製藥廠商查獲一百一十六萬顆假藥,包括假威而鋼、犀利士和減肥產品等,其中台北市調查處更搜出超過九十二萬顆「保健膠囊」,估計市值近千萬元新台幣(約二百五十萬港元)。
懷疑製假藥的廠商名為「三合興業藥業公司」,調查人員指它在所謂的「保健膠囊」攙入銀杏葉萃取物,並以「保健為主、多吃無害」宣傳手法銷售,產品包括「納豆酵素膠囊」、「納豆菌軟膠囊」、「白果錠」、「藍莓素」、「葉黃素軟膠囊」、「姬松茸軟膠囊」等,聲稱服用後可改善血液循環、增強記憶力,惟產品來源可疑。
台檢獲15公噸假中藥粉
台灣衞生署指,銀杏葉萃取物可引起皮膚過敏、頭痛、胃腸出血等,糖尿病和高血壓病患者服食可導致腎衰竭。若與抗血小板藥物一同服食,有機會導致大量出血,小童和孕婦不宜服用。
另外,台灣雲林縣亦揭發有非法工場「大益中藥製造工廠」製造假中藥粉,並遭檢獲十五公噸中藥粉。工場內只見大批黑色中藥丸散置在塑膠盒內,「製藥」工人則在趕工,甫見調查人員顯得慌張失措。
事實上,去年十一月亦發現在本港發售的台灣生產中成藥產品被驗出重金屬超標。本港衞生署公布顯示,該產品聲稱可去瘀,但鉛含量超出標準上限,要求該產品的本港批發商回收有問題的產品。

本港中成藥種類繁多,市民宜小心選購。
港對保健產品抽查不足
香港醫院藥劑師學會副會長崔俊明指出,本港對於「保健產品」的監管不足,「呢類產品種類繁多,因為多數係天然食品中抽取物質,目前冇得監管,亦好難監管,只能靠政府去抽查。」但他直言,現時的抽查多局限在檢驗產品的品質問題,包括是否攙入西藥成分或污染物。他提醒市民勿把所謂的保健產品當成藥物般治療疾病,「好似銀杏葉聲稱可以紓緩老人癡呆症,但外國研究已發現根本對個病冇幫助。」他建議,市民服用任何保健產品前應諮詢醫生意見,留意是否與自己服用的藥物相沖,購買時亦要光顧有信譽的商舖。
本港藥物多從外地進口,統計處資料顯示,去年進口本港的醫療及藥用產品總值高達一百四十二億元。
根據《中醫藥條例》,凡符合中成藥定義的產品必須向中醫藥管理委員會轄下的中藥組註冊申請,才可進口、在本港製造和銷售;而每批進口的中成藥亦要按《進出口條例》規定,進口前必須取得由衞生署署長發出的許可證,以及符合基本的安全要求。
本港衞生署發言人回覆本報查詢稱,就台灣是次黑心「保健產品」問題,該署將與台灣當局了解事件。

保濟丸被驗出禁藥而需要回收,事件引發中成藥監管問題。
保濟丸事件 衞署反應遲鈍
台灣行政院長吳敦義一聲令下嚴打假藥,即時搜查廿三間藥廠,查獲逾百萬顆來歷不明的黑心膠囊,數量龐大,顯示當局打擊假藥的決心。反觀香港卻「歎慢板」,自上月八日新加坡政府回收問題保濟丸後,事隔逾兩星期,本港衞生署才採取回收行動,五日後方宣布巡查全港約五百間藥廠。
進口中成藥 無即時化驗
自問題保濟丸被揭流入本港,衞生署遲遲未有交代原因。其實現時進口本港的中成藥,署方毋須即時化驗,僅審批藥廠提交的化驗報告,藥物獲註冊後,才抽查覆核樣本或對投訴藥物進行化驗。
去年署方檢驗約五千一百個產品樣本,包括西藥、中成藥和健康產品,其中約百分之一點五的樣本被驗出不合格或不符合標準,部分是市民從外地購買及服用後不適送院而發現。當中有十七宗被檢控,其中三宗已被定罪,罰款由四千元至一萬五千元不等;五宗遭警告,另有九宗仍在處理中。
GMP規範中成藥港僅七藥廠達標
近年世界各地對中成藥的質量愈趨關注,並且主動加強對中成藥藥廠的監管,台灣及內地都已強制執行「中成藥生產質量管理規範」(GMP),但本港直至近日保濟丸事件後,才後知後覺加強巡查。
確保產品質素
GMP是一套對中成藥生產質量管理的規範,對品質控制、廠房設計、員工衞生、文件處理及驗證等,都有嚴格規管,以確保產品質素。
二○○四年,內地國家食品藥品監督管理局要求各省級藥品監督管理部門嚴格執法,對未通過GMP認證的藥品生產企業,實施停產或注銷許可證,如發現應該停產而沒有停產的企業亦要依法查處。
而已經取得內地GMP的企業,亦要按要求每年檢查一次,未符合GMP標準的要按照規定處理。
台灣更早於一九八二年已公告GMP制度,全部藥廠並於二○○三年完成認證,原本一百二十八間中藥廠中只有二十八間符合GMP的標準;二○○六年十月一日起,未取得當地合法認證的中成藥均不可以出售。
相反,本港現時約有五百間中成藥製造商,當中只有七間達GMP標準,並且在爆出保濟丸事件後才加強巡查。

本港目前只有七間藥廠符合GMP標準。

○四年,內地國家食品藥品監督管理局執行GMP,對藥廠有嚴格要求。

台調查局分別查獲一百一十六萬顆黑心膠囊及十五公噸偽中藥粉末。 (本報台北傳真)
台灣衞生署食品藥物管理局表示,近日在全台展開偽藥行動,並於二十三家製藥廠商查獲一百一十六萬顆假藥,包括假威而鋼、犀利士和減肥產品等,其中台北市調查處更搜出超過九十二萬顆「保健膠囊」,估計市值近千萬元新台幣(約二百五十萬港元)。
懷疑製假藥的廠商名為「三合興業藥業公司」,調查人員指它在所謂的「保健膠囊」攙入銀杏葉萃取物,並以「保健為主、多吃無害」宣傳手法銷售,產品包括「納豆酵素膠囊」、「納豆菌軟膠囊」、「白果錠」、「藍莓素」、「葉黃素軟膠囊」、「姬松茸軟膠囊」等,聲稱服用後可改善血液循環、增強記憶力,惟產品來源可疑。
台檢獲15公噸假中藥粉
台灣衞生署指,銀杏葉萃取物可引起皮膚過敏、頭痛、胃腸出血等,糖尿病和高血壓病患者服食可導致腎衰竭。若與抗血小板藥物一同服食,有機會導致大量出血,小童和孕婦不宜服用。
另外,台灣雲林縣亦揭發有非法工場「大益中藥製造工廠」製造假中藥粉,並遭檢獲十五公噸中藥粉。工場內只見大批黑色中藥丸散置在塑膠盒內,「製藥」工人則在趕工,甫見調查人員顯得慌張失措。
事實上,去年十一月亦發現在本港發售的台灣生產中成藥產品被驗出重金屬超標。本港衞生署公布顯示,該產品聲稱可去瘀,但鉛含量超出標準上限,要求該產品的本港批發商回收有問題的產品。

本港中成藥種類繁多,市民宜小心選購。
港對保健產品抽查不足
香港醫院藥劑師學會副會長崔俊明指出,本港對於「保健產品」的監管不足,「呢類產品種類繁多,因為多數係天然食品中抽取物質,目前冇得監管,亦好難監管,只能靠政府去抽查。」但他直言,現時的抽查多局限在檢驗產品的品質問題,包括是否攙入西藥成分或污染物。他提醒市民勿把所謂的保健產品當成藥物般治療疾病,「好似銀杏葉聲稱可以紓緩老人癡呆症,但外國研究已發現根本對個病冇幫助。」他建議,市民服用任何保健產品前應諮詢醫生意見,留意是否與自己服用的藥物相沖,購買時亦要光顧有信譽的商舖。
本港藥物多從外地進口,統計處資料顯示,去年進口本港的醫療及藥用產品總值高達一百四十二億元。
根據《中醫藥條例》,凡符合中成藥定義的產品必須向中醫藥管理委員會轄下的中藥組註冊申請,才可進口、在本港製造和銷售;而每批進口的中成藥亦要按《進出口條例》規定,進口前必須取得由衞生署署長發出的許可證,以及符合基本的安全要求。
本港衞生署發言人回覆本報查詢稱,就台灣是次黑心「保健產品」問題,該署將與台灣當局了解事件。

保濟丸被驗出禁藥而需要回收,事件引發中成藥監管問題。
保濟丸事件 衞署反應遲鈍
台灣行政院長吳敦義一聲令下嚴打假藥,即時搜查廿三間藥廠,查獲逾百萬顆來歷不明的黑心膠囊,數量龐大,顯示當局打擊假藥的決心。反觀香港卻「歎慢板」,自上月八日新加坡政府回收問題保濟丸後,事隔逾兩星期,本港衞生署才採取回收行動,五日後方宣布巡查全港約五百間藥廠。
進口中成藥 無即時化驗
自問題保濟丸被揭流入本港,衞生署遲遲未有交代原因。其實現時進口本港的中成藥,署方毋須即時化驗,僅審批藥廠提交的化驗報告,藥物獲註冊後,才抽查覆核樣本或對投訴藥物進行化驗。
去年署方檢驗約五千一百個產品樣本,包括西藥、中成藥和健康產品,其中約百分之一點五的樣本被驗出不合格或不符合標準,部分是市民從外地購買及服用後不適送院而發現。當中有十七宗被檢控,其中三宗已被定罪,罰款由四千元至一萬五千元不等;五宗遭警告,另有九宗仍在處理中。
GMP規範中成藥港僅七藥廠達標
近年世界各地對中成藥的質量愈趨關注,並且主動加強對中成藥藥廠的監管,台灣及內地都已強制執行「中成藥生產質量管理規範」(GMP),但本港直至近日保濟丸事件後,才後知後覺加強巡查。
確保產品質素
GMP是一套對中成藥生產質量管理的規範,對品質控制、廠房設計、員工衞生、文件處理及驗證等,都有嚴格規管,以確保產品質素。
二○○四年,內地國家食品藥品監督管理局要求各省級藥品監督管理部門嚴格執法,對未通過GMP認證的藥品生產企業,實施停產或注銷許可證,如發現應該停產而沒有停產的企業亦要依法查處。
而已經取得內地GMP的企業,亦要按要求每年檢查一次,未符合GMP標準的要按照規定處理。
台灣更早於一九八二年已公告GMP制度,全部藥廠並於二○○三年完成認證,原本一百二十八間中藥廠中只有二十八間符合GMP的標準;二○○六年十月一日起,未取得當地合法認證的中成藥均不可以出售。
相反,本港現時約有五百間中成藥製造商,當中只有七間達GMP標準,並且在爆出保濟丸事件後才加強巡查。

本港目前只有七間藥廠符合GMP標準。

○四年,內地國家食品藥品監督管理局執行GMP,對藥廠有嚴格要求。

p-ma- 文章數 : 956
注冊日期 : 2009-12-02
 服瀉肝丸致癌 英擬中醫登記制
服瀉肝丸致癌 英擬中醫登記制
英國擬要求當地所有中醫師進行登記,以加強中醫藥規管。早前一名自稱為中醫的華裔女子向病人售賣含禁藥的中成藥瀉肝丸,導致病人腎衰竭及患癌,引起中醫藥缺乏規管的廣泛關注。但有中醫組織大潑冷水,認為負責的委員會並無足夠的規管能力。
英國《每日郵報》報道,英國衞生大臣貝安德表示,當局將收緊法例,要求所有當地中醫師到補充及自然療法委員會(Complementary and Natural Healthcare Council,CNHC)登記註冊,以加強監管中醫藥,有接近二千五百名中醫將首當其衝受到影響。政府稍後會向專業團體和地方政府進行諮詢,至於針灸會否被納入規管範圍則未有定案。
歐洲草藥及傳統中醫藥人員聯會(EHTPA)指,CHNC只是一個自願性組織,缺乏人手、資源及法定地位,因此當局所講的規管計劃只是逃避的藉口。
聯會主席麥金太爾說:「中醫應像其他執業醫療人士般,受到法例監管,否則蒙受損失的只會是公眾。」
自稱在中國是一名合資格中醫,但在英國並無行醫執照的華裔女子吳英(譯音)今年二月承認,自一九九七年起向五十八歲公務員布思(Patricia Booth)出售含馬兜鈴酸(Aristolochic acid)的中藥「瀉肝丸」,聲稱可治療其面部皮膚問題。其時馬兜鈴酸需由持牌醫生處方,之後被列為禁藥。
公僕中招患尿道癌
布思在五年內每天服用三次「瀉肝丸」,導致健康變差,出現腎衰竭及患上尿道癌。法官最終判吳英守行為兩年,並且批評政府缺乏對中醫藥的監管。
英國《每日郵報》報道,英國衞生大臣貝安德表示,當局將收緊法例,要求所有當地中醫師到補充及自然療法委員會(Complementary and Natural Healthcare Council,CNHC)登記註冊,以加強監管中醫藥,有接近二千五百名中醫將首當其衝受到影響。政府稍後會向專業團體和地方政府進行諮詢,至於針灸會否被納入規管範圍則未有定案。
歐洲草藥及傳統中醫藥人員聯會(EHTPA)指,CHNC只是一個自願性組織,缺乏人手、資源及法定地位,因此當局所講的規管計劃只是逃避的藉口。
聯會主席麥金太爾說:「中醫應像其他執業醫療人士般,受到法例監管,否則蒙受損失的只會是公眾。」
自稱在中國是一名合資格中醫,但在英國並無行醫執照的華裔女子吳英(譯音)今年二月承認,自一九九七年起向五十八歲公務員布思(Patricia Booth)出售含馬兜鈴酸(Aristolochic acid)的中藥「瀉肝丸」,聲稱可治療其面部皮膚問題。其時馬兜鈴酸需由持牌醫生處方,之後被列為禁藥。
公僕中招患尿道癌
布思在五年內每天服用三次「瀉肝丸」,導致健康變差,出現腎衰竭及患上尿道癌。法官最終判吳英守行為兩年,並且批評政府缺乏對中醫藥的監管。

B-52- 訪客
 山寨中藥廠350間未達標
山寨中藥廠350間未達標
本港約有五百間中成藥製造商之中,多達三百五十間只持過渡性註冊,衞生署去年底完成巡查此類藥廠,發現全部不達標。有三十間處所的環境不理想需搬遷外,多達二百五十間因未能防止藥物受污染等問題導致生產環境未達標。衞生署至今仍未定出明確的改善期限,只稱希望一至兩年內可「處理咗佢」,允許未達標的「山寨廠」生產的中成藥繼續通街賣。關注團體炮轟衞生署拖得就拖,促請當局定下時間表,盡快結束過渡期。

本港三百五十間中成藥製造商,仍然屬於過渡性註冊。
全部持過渡性牌照
衞生署助理署長趙佩燕表示,去年底完成巡查三百五十間持過渡性牌照的中成藥製造商,三十間的處所環境不理想,如位於住宅大廈內,需要搬遷及暫時停產;二百五十間的生產環境需要改善,包括未能防止藥物受污染、技術及人手等問題,或申請正式牌照的資料需進一步補充等。其餘七十間已經結業或向衞生署提出取消正式註冊申請。共有十一個持過渡性牌照的中成藥廠申請正式牌照被拒。
趙佩燕未有表態何時結束過渡期,只呼籲未達標的藥廠考慮結業,「希望一至兩年內將過渡性註冊中藥廠處理咗佢。」她說,署方長遠希望中成藥製造商達西藥的GMP(生產質量管理規範)標準,但中成藥製造歷史悠久,仍有很多問題未解決,未有達致GMP標準的時間表。
《中醫藥條例》容許過渡性領牌,除非中成藥製造商的正式牌照申請被拒,或食物及衞生局決定結束過渡期,否則即使藥廠未達標,仍可繼續生產藥物。
縱容差劣如罰正牌
全民健康動力主席勞永樂批評,條例○三年實施至今已經七年,「政府最多只可畀多三年時間中成藥業界,如果間廠十年都改善唔到,即係永遠都改唔到!」他指市民難以分辨市面上的中成藥由哪些藥廠出品,「咁樣縱容唔達標嘅廠,等如懲罰達標嘅!」
○三年底至今年三月底,衞生署中藥組共收到逾一萬六千宗中成藥註冊申請,但署方○九年全年僅化驗一百五十七個中成藥樣本,當中三個被驗出重金屬含量超標。至於李眾勝堂的膠囊裝保濟丸被驗出含致癌藥,衞生署仍跟進中,完成調查後會諮詢律政司意見,考慮提出檢控。

本港三百五十間中成藥製造商,仍然屬於過渡性註冊。
全部持過渡性牌照
衞生署助理署長趙佩燕表示,去年底完成巡查三百五十間持過渡性牌照的中成藥製造商,三十間的處所環境不理想,如位於住宅大廈內,需要搬遷及暫時停產;二百五十間的生產環境需要改善,包括未能防止藥物受污染、技術及人手等問題,或申請正式牌照的資料需進一步補充等。其餘七十間已經結業或向衞生署提出取消正式註冊申請。共有十一個持過渡性牌照的中成藥廠申請正式牌照被拒。
趙佩燕未有表態何時結束過渡期,只呼籲未達標的藥廠考慮結業,「希望一至兩年內將過渡性註冊中藥廠處理咗佢。」她說,署方長遠希望中成藥製造商達西藥的GMP(生產質量管理規範)標準,但中成藥製造歷史悠久,仍有很多問題未解決,未有達致GMP標準的時間表。
《中醫藥條例》容許過渡性領牌,除非中成藥製造商的正式牌照申請被拒,或食物及衞生局決定結束過渡期,否則即使藥廠未達標,仍可繼續生產藥物。
縱容差劣如罰正牌
全民健康動力主席勞永樂批評,條例○三年實施至今已經七年,「政府最多只可畀多三年時間中成藥業界,如果間廠十年都改善唔到,即係永遠都改唔到!」他指市民難以分辨市面上的中成藥由哪些藥廠出品,「咁樣縱容唔達標嘅廠,等如懲罰達標嘅!」
○三年底至今年三月底,衞生署中藥組共收到逾一萬六千宗中成藥註冊申請,但署方○九年全年僅化驗一百五十七個中成藥樣本,當中三個被驗出重金屬含量超標。至於李眾勝堂的膠囊裝保濟丸被驗出含致癌藥,衞生署仍跟進中,完成調查後會諮詢律政司意見,考慮提出檢控。

hkinca38- 訪客
 醫管局中藥測試不足
醫管局中藥測試不足
醫院管理局除了去年被揭發,向病人供應含毛霉菌西藥外,原來對中成藥及中藥材亦缺乏監管。過去兩個年度,該局只就 230種中藥進行測試,佔該局使用的中藥半數,明顯不足。 08/09至 09/10年度該局接獲配藥員提出 100宗中藥材質素問題的投訴。
兩年度員工投訴百宗
該局醫療服務發展委員會文件指出,所有向醫管局供應中藥,如中成藥顆粒及經加工的中藥材,均來自獲 GMP認證藥廠。但該局承認,自 05年起就中藥進行的安全性及藥物成份是否符合標準的測試,屬很小規模; 08年起測試樣本數目及規模增加,若中藥材本身有毒性、容易與其他藥材混淆,及容易被假冒的昂貴中藥,屬優先化驗。
08/09至 09/10年度醫管局只測試了 230款中藥,佔該局使用的中藥數量約一半,但有關中藥的價值佔該局中藥總開支約 80%。
該局為確保藥廠送來的中藥合乎標準,設有投訴及回收機制。 08/09至 09/10年度該局接獲配藥員提出 100宗,有關中藥材質素問題的投訴。投訴包括中藥材含西藥成份;生產過程有問題;中藥材分解出問題如水份流失及出油,甚至是假貨。局方就所有投訴進行調查。
該局指出,最近加入多種不同中藥測試,如重金屬、殘餘農藥、微生物含量。部份中藥材更要測試污染物含量及毒性。現時不少市民有服食中藥習慣,自 04年後該局接獲 420宗服食中藥引致不良反應報告,每年增加兩成。本年度該局會設立一個獨立中藥不良反應報告系統,進一步監察及分析個案。
兩年度員工投訴百宗
該局醫療服務發展委員會文件指出,所有向醫管局供應中藥,如中成藥顆粒及經加工的中藥材,均來自獲 GMP認證藥廠。但該局承認,自 05年起就中藥進行的安全性及藥物成份是否符合標準的測試,屬很小規模; 08年起測試樣本數目及規模增加,若中藥材本身有毒性、容易與其他藥材混淆,及容易被假冒的昂貴中藥,屬優先化驗。
08/09至 09/10年度醫管局只測試了 230款中藥,佔該局使用的中藥數量約一半,但有關中藥的價值佔該局中藥總開支約 80%。
該局為確保藥廠送來的中藥合乎標準,設有投訴及回收機制。 08/09至 09/10年度該局接獲配藥員提出 100宗,有關中藥材質素問題的投訴。投訴包括中藥材含西藥成份;生產過程有問題;中藥材分解出問題如水份流失及出油,甚至是假貨。局方就所有投訴進行調查。
該局指出,最近加入多種不同中藥測試,如重金屬、殘餘農藥、微生物含量。部份中藥材更要測試污染物含量及毒性。現時不少市民有服食中藥習慣,自 04年後該局接獲 420宗服食中藥引致不良反應報告,每年增加兩成。本年度該局會設立一個獨立中藥不良反應報告系統,進一步監察及分析個案。

hkinca38- 訪客
 藥物事故 曾食死人
藥物事故 曾食死人
近年藥物事故接二連三發生,激發帳委會罕有地譴責食物及衞生局和衞生署。自去年初歐化藥業生產的痛風藥別嘌醇含菌食死人後,當局成立藥物監管制度檢討委員會,提出七十五項改善建議,可惜建議大部分未落實,又爆出中成藥及西藥品質事故,除百年老字號李眾勝堂保濟丸被驗出含減肥藥及致癌成分需全港回收外,嘉琳製藥廠更因藥物未能通過分解測試而要回收全廠藥物。
歐化藥業生產的痛風藥別嘌醇,去年被揭發受毛霉菌污染,導致最少八名癌症病人死亡。藥物監管制度檢討委員會商討九個月後提交建議書,不過大部分建議如要求持「良好藥品生產規範」(GMP)的藥廠提升至歐盟的PICS水平,均要六至十年時間去執行,被藥劑業界批評遠水不能救近火。
未註冊中成藥隨街買到
除西藥出問題外,今年三月李眾勝堂保濟丸輕便裝被新加坡驗出含致癌藥「酚酞」和減肥藥「西布曲明」,本港衞生署待新加坡回收才知悉藥物出事,顯示當局後知後覺,亦再次令人關注中成藥遲遲未有監管,導致未註冊及品質成疑的中成藥在街上隨便可以買到。
藥物事故似乎未有停下來,今年四月底澳門驗出持香港GMP牌照的嘉琳製藥廠藥物有問題,上月初衞生署抽查時才發現嘉琳十三種藥物未能通過藥物分解測試,或藥物成分少於註冊分量,可能令到病人服藥後無效,或產生細菌抗藥性。
嘉琳被衞生署飭令從市面回收全廠生產的四百三十四款藥物,掀起史無前例的大規模回收行動。
歐化藥業生產的痛風藥別嘌醇,去年被揭發受毛霉菌污染,導致最少八名癌症病人死亡。藥物監管制度檢討委員會商討九個月後提交建議書,不過大部分建議如要求持「良好藥品生產規範」(GMP)的藥廠提升至歐盟的PICS水平,均要六至十年時間去執行,被藥劑業界批評遠水不能救近火。
未註冊中成藥隨街買到
除西藥出問題外,今年三月李眾勝堂保濟丸輕便裝被新加坡驗出含致癌藥「酚酞」和減肥藥「西布曲明」,本港衞生署待新加坡回收才知悉藥物出事,顯示當局後知後覺,亦再次令人關注中成藥遲遲未有監管,導致未註冊及品質成疑的中成藥在街上隨便可以買到。
藥物事故似乎未有停下來,今年四月底澳門驗出持香港GMP牌照的嘉琳製藥廠藥物有問題,上月初衞生署抽查時才發現嘉琳十三種藥物未能通過藥物分解測試,或藥物成分少於註冊分量,可能令到病人服藥後無效,或產生細菌抗藥性。
嘉琳被衞生署飭令從市面回收全廠生產的四百三十四款藥物,掀起史無前例的大規模回收行動。

KateBush- 訪客
 未註冊中成藥年底規管
未註冊中成藥年底規管
中成藥註冊制度已實施六年多,中醫藥管理委員會接獲一萬六千多宗申請,但其中四千多種中成藥至今未能提交基本的安全測試報告,連臨時性質的過渡性註冊要求也達不到。這些品質成疑的中成藥充斥市面,出售並不違法。藥物監管工作一團糟的衞生署,最近突然向中成藥製造商發出「最後通牒」,表示將於下月向立法會提交禁止未註冊中成藥製造或銷售的條文,目標為今年十二月一日起生效。業界不滿不足一個月的諮詢期今日結束,有「夾硬嚟」之嫌。
中醫藥管理委員會中藥組○三年尾開始接受中成藥註冊申請,截至今年四月收到一萬六千五百多宗申請,有二千一百宗屬非過渡性註冊中成藥(HKNT),即藥物自九九年三月之後供應,已交齊包括重金屬、有毒元素、農藥殘留量及微生物報告。另有九千一百多宗在九九年三月之前銷售的中成藥,亦能提交所需化驗報告,獲過渡性註冊(HKP)。
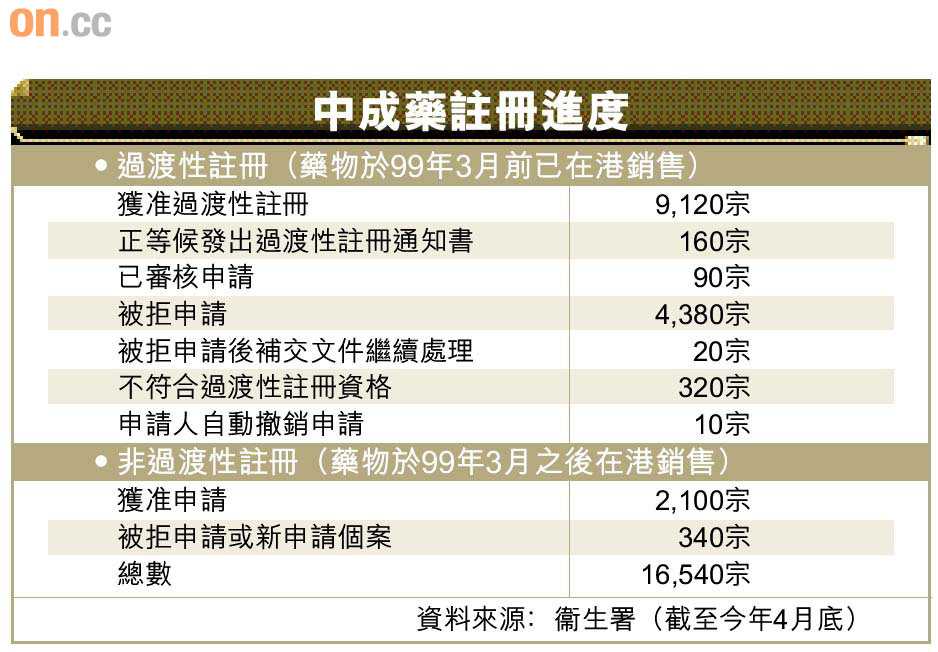
衞生署計劃本年底全面實施規管未註冊中成藥條文,凡進口、銷售、管有或製造未經註冊的中成藥即屬違法,最高刑罰為罰款十萬元和監禁兩年。該署希望立法會在七月至十一月期間考慮有關條文和刊憲後,於十二月一日起生效。中成藥標籤及說明書要求的條文則建議於明年十二月一日起才生效。
業界未消化文件內容
香港中成藥商會會長丁志輝認為,中成藥註冊實施多年,已給予業界足夠時間提交註冊所需的各項安全測試,已到適當時候規管中成藥銷售和實施有關罰則。業界希望條例愈快實施愈好,「無理由咁耐以來又唔註冊,又喺市面賣,咁對守法嘅業界唔公平」。
香港藥行商會理事長黃炳明則指,諮詢期由五月廿六日開始,中藥組於五月卅一日業界簡介會中,只交代條文內容,並未交代生效時間。諮詢文件延至本月才發出,業界未消化文件內容,諮詢期今日結束,批評衞生署假諮詢。
倉卒立法 漏洞難補救
醫療政策評議會發言人郭家麒表示,規管中成藥的法例早已經存在,但遲遲未正式實施,令未註冊中成藥「無王管」,衞生署應盡快將有關條例交立法會。但他同意諮詢期太短,不但對業界不公平,消費者、病人組織和藥劑師組織等都沒有時間看清楚條文,令他們無法表達意見,日後實施時才發現漏洞就難以補救。
記者蘇家欣
中醫藥管理委員會中藥組○三年尾開始接受中成藥註冊申請,截至今年四月收到一萬六千五百多宗申請,有二千一百宗屬非過渡性註冊中成藥(HKNT),即藥物自九九年三月之後供應,已交齊包括重金屬、有毒元素、農藥殘留量及微生物報告。另有九千一百多宗在九九年三月之前銷售的中成藥,亦能提交所需化驗報告,獲過渡性註冊(HKP)。

衞生署計劃本年底全面實施規管未註冊中成藥條文,凡進口、銷售、管有或製造未經註冊的中成藥即屬違法,最高刑罰為罰款十萬元和監禁兩年。該署希望立法會在七月至十一月期間考慮有關條文和刊憲後,於十二月一日起生效。中成藥標籤及說明書要求的條文則建議於明年十二月一日起才生效。
業界未消化文件內容
香港中成藥商會會長丁志輝認為,中成藥註冊實施多年,已給予業界足夠時間提交註冊所需的各項安全測試,已到適當時候規管中成藥銷售和實施有關罰則。業界希望條例愈快實施愈好,「無理由咁耐以來又唔註冊,又喺市面賣,咁對守法嘅業界唔公平」。
香港藥行商會理事長黃炳明則指,諮詢期由五月廿六日開始,中藥組於五月卅一日業界簡介會中,只交代條文內容,並未交代生效時間。諮詢文件延至本月才發出,業界未消化文件內容,諮詢期今日結束,批評衞生署假諮詢。
倉卒立法 漏洞難補救
醫療政策評議會發言人郭家麒表示,規管中成藥的法例早已經存在,但遲遲未正式實施,令未註冊中成藥「無王管」,衞生署應盡快將有關條例交立法會。但他同意諮詢期太短,不但對業界不公平,消費者、病人組織和藥劑師組織等都沒有時間看清楚條文,令他們無法表達意見,日後實施時才發現漏洞就難以補救。
記者蘇家欣

hkinca38- 訪客
INCA's forum :: 純聊天, 八卦, 資訊交流 :: 醫療康健
第1頁(共2頁)
這個論壇的權限:
您 無法 在這個版面回復文章



» 【特寫】踢拖抗暴 — 當催淚彈蔓延至長者社區.黃大仙黑夜
» 【8.4 將軍澳遊行】寶琳站黑衣人潮湧現 有商場謝絕警方內進
» 【8.4 港島示威 ‧ 不斷更新】警石塘咀放催淚彈 示威者轉戰銅鑼灣 快閃封紅隧
» 【8-3 旺角遊行】歷幾許衝突士多照開舖 老闆:佔旺時無破壞有幫襯
» 香港青年對英殖時期的「懷念」從何而來?
» 【暴動罪審訊】譴責暴動罪檢控 民權觀察促政府回應訴求 (12:49)
» 【CBD】大麻萃取物產品層出不窮 是神奇草藥抑或要有更多監管
» 點解八月五號要罷工?